宇宙航空研究開発機構(JAXA)の動物実験計画書の審査に質問書
宇宙航空研究開発機構(JAXA)のウェブサイトで公開されている動物実験委員会の議事録の中に審査結果の概要が記載されていますが、問題等を指摘しつつもそのまま承認としている箇所が散見されたため、質問書を送付しました。
問題等が是正されないまま実験が実施されたのではないかとの懸念を持ちましたが、回答としては、「再審議が行われていたが議事録上それが読み取れなかったので改善する」というのが主旨です。
回答の中に質問も含まれていますので、長文ですが、全文まるごと掲載いたします。
※ただし、ブラウザ上での読みやすさを考え、段落間に改行を入れました。
また、注釈として参考となる情報へリンクを張っています。
参考:
平成 28 年 2 月 29 日
PEACE~命の搾取ではなく尊厳を
代表 東 さちこ 様
国立研究開発法人 宇宙航空研究開発機構
「質問書」に対する回答
このたびは、国立研究開発法人宇宙航空研究開発機構(JAXA)の事業内容につきましてご関心とご質問を賜り御礼申し上げます。
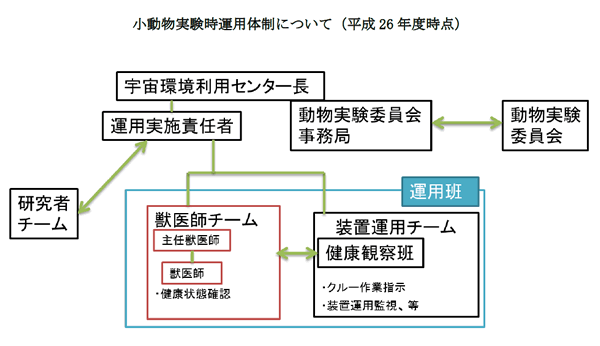
JAXA では、関連法令、基準、指針ならびに国際的なガイドライン等に則り、JAXA 動物実験委員会において実験計画書を審査し、最終的に JAXA 理事長が承認しております。JAXA 動物実験委員会で承認されなかった実験計画書(条件付承認を含む)については、当該実験責任者に指摘事項を伝え、再提出された実験計画書を再度 JAXA 動物実験委員会が審査した上で JAXA 理事長が実験計画書を承認しております。
2016 年 2 月 9 日付「動物実験計画書の審査に関する質問書」でお問い合わせいただきました内容につきましては、JAXA ウェブサイトにおいて公開しております議事録において、議事録記載時点(委員会開催時点)で条件付承認となった案件に関しまして、その後の JAXA 動物実験委員会における再審議経過等が未記載であったため、ご懸念いただくこととなり申し訳ございませんでした。
今後は、このたびご指摘いただきました事項に鑑み、議事録への再審議経過等の記載方法についても工夫し、誤解を招かないようにいたしたいと考えております。
ご質問につきましては、以下のとおり回答いたします。
今後ともよろしくお願い申し上げます。
Ⅰ.第 25 回宇宙航空研究開発機構動物実験委員会議事録(平成 27 年 3 月 6 日)について
回答:本件は、JAXA 職員が動物実験を行うものではありませんでしたので、審査対象外としました。本実験は、他機関で動物実験及びその審査が行われており、JAXA 職員は当該機関ですでに行われた動物実験のデータを用いて、データ解析のみを担当することを JAXA 動物実験委員会にて確認しています。今後は、審査対象外とした理由を議事録に明記するよう改善を図ります。
なお、JAXA 動物実験委員会の審査対象となる実験計画の範囲につきましては、別紙 1 の「1. JAXA 動物実験委員会の審査対象範囲」をご参照ください。
回答: JAXA 動物実験委員会は、すべての実験計画書について、動物の苦痛の軽減を含めて3R の観点から審査を行っています。
本件においては、提出された実験計画書に医薬品レベル以外の麻酔薬の使用の記載がありましたので、JAXA 動物実験委員会より「医薬品レベルの麻酔薬の使用を推奨する」旨のコメントを当該機関の実験責任者に伝えました。なお、コメント通達後、当該実施機関にて麻酔薬が医薬品レベルのものに変更されたことを JAXA 動物実験委員会では確認しております。
今後、議事録においてコメントの対応結果を明記するよう改善を図ります。
他機関における動物実験委員会にて審議された実験計画の取り扱いについては、別紙 1 の「1.JAXA 動物実験委員会の審査対象範囲」をご参照ください。
Ⅱ.第 24 回宇宙航空研究開発機構動物実験委員会議事録(平成 26 年 12 月 4 日)について
これらの文章から、代替法が検討されないまま、実験計画が承認されたことがわかります。また、「代替できない」という結論ありきで、ただ単に記述を求めるのは、実験計画書の審査のあり方として、間違っているのではないでしょうか。そもそも、なぜ新規物質の毒性評価を「きぼう」で行う必要があるのですか。 確かにドレイズ法は OECD のテストガイドラインからもまだ削除はされていませんが、まず代替法を用い、その結果によってドレイズ法を用いる2段階になってきているかと思います。まず代替法を用いるようコメントしなかったのはどうしてですか。また、このテストは、2012 年に改定された新 OECD TG405 に従った方法で行われていますか。
回答:「条件付承認」は、JAXA 動物実験委員会で指摘された条件に対し、実験責任者が条件を満たすよう実験計画を見直した上で再提出し、JAXA 動物実験委員会で条件への適正な対応がなされていることを確認した後でなければ実験を始めることはできません。JAXA 動物実験委員会での承認等の取り扱いについては、別紙 1 の「2. 承認等の取り扱いについて」をご参照ください。
JAXA 動物実験委員会は「きぼう」での実験だけでなく、JAXA 全体として、地上で実施している動物実験も対象としています。本件は、宇宙機の推進薬の新規開発に係る地上での実験であり、「きぼう」で行う実験ではありません。従来の推進薬は毒性が高いため、JAXA では、作業性向上、取扱い手順の簡素化等を目指し、新規に毒性の低い推進薬の開発に取り組んでおり、本実験計画はその毒性評価を目的としたものです。
上記条件(代替法が使用できるか確認すること)に対しては、毒物指定・劇物指定の判定は「毒物劇物の判定基準(厚生労働省:平成 19 年 3 月改正)」に基づく必要があり、本基準においてドレイズ試験の実施が具体的に指定されていることから、ドレイズ法の実施が必要(代替法が不可)である旨、実験責任者からの回答を受領しています。
本回答について、再度 JAXA 動物実験委員会で審議を行い、条件への適正な対応がなされていることを確認した上で、本実験計画書を承認いたしました。なお、実験は OECD テストガイドライン 405 に準拠していることも、承認前に確認しています。今後、議事録において条件への対応を明記するよう改善を図ります。
Ⅲ.第 22 回宇宙航空研究開発機構動物実験委員会議事録(平成 26 年 6 月 3 日)について
回答:条件付承認の取り扱いについては、ご質問Ⅱ(1)への回答及び別紙 1 の「2. 承認等の取り扱いについて」をご参照ください。
本件は、宇宙からの帰還時にマウスの環境制御機能に突発的に不具合が生じた場合を想定して計画されたものです。
JAXA 動物実験委員会による上記条件に対して、実験責任者より、25℃の体温でマウスの生存を示す文献「実験動物の環境と管理(山内忠平著、アドスリー、2008 年)」に基づき、人道的エンドポイントを設定した旨の回答を受領しています。
本回答について、再度 JAXA 動物実験委員会で審議を行い、条件への適正な対応がなされていることを確認した上で、本実験計画書を承認いたしました。今後、議事録において条件への対応を明記するよう改善を図ります。
なお、本実験計画は、動物実験施設の条件設定が困難であることが判明したため、未実施であることが報告されています。
Ⅳ.第 21 回宇宙航空研究開発機構動物実験委員会議事録(平成 26 年 3 月 10 日)について
回答:条件付承認の取り扱いについては、ご質問Ⅱ(1)への回答及び別紙 1 の「2. 承認等の取り扱いについて」をご参照ください。
本件については、実験計画書において、代替法について検討したが代替不可能であることが記載されていましたが、具体的な検討方法(Medline 等で検索したか、その他の方法か)が未記載であったため、JAXA 動物実験委員会より指摘し、再提出を求めたものです。また、実験動物数を決定した理由についても、具体的に記載することを指示しました。
上記指摘に対して、実験責任者から修正された実験計画書が提出され、再度 JAXA 動物実験委員会が審議を行いました。条件への適正な対応がなされていることを確認した上で、本実験計画書を承認いたしました。今後、議事録において条件への対応を明記するよう改善を図ります。
回答:上記コメントは、JAXA 動物実験委員会の事前審査担当委員により、JAXA 動物実験委員会開催前に予め提出された実験計画書に対する指導コメントであり、動物実験委員会開催前に実験責任者に伝えられました。
JAXA 動物実験委員会開催時点では、本事前指導コメントを反映・修正した実験計画書が委員会に提出され、委員会の場で適正であることが判断されたため、承認いたしました。今後、事前指導コメントについては議事録においてその旨明記する等改善を図ります。
回答:本件は、実験計画書のチェック項目箇所の誤りに対する指摘です。
代替法の検討方法についてのチェック箇所が、「その他」にチェックの上、「文献等で検索」と記載されていましたが、文献等で検索した場合は、「その他」ではなく「Medline 等で検索」欄が正しいチェック箇所であるため、修正を指示したものです。今後、議事録において誤記等であることを明記するよう改善を図ります。
Ⅴ.その他
回答:実験責任者に対し、毎年一回、実験終了後の報告書提出を義務付けています。また、JAXA 動物実験委員会で、提出された報告内容について、問題の有無を確認しています。
回答:本資料については公開しておりません。内容については別紙2に添付いたします。
別紙 1
JAXA 動物実験委員会における審査について
JAXA 動物実験委員会では、JAXA の資産(職員・施設・資金を含む)を使用し実施する研究、試験、及び教育、ならびに装置開発等における業務のうち、ほ乳類、鳥類、爬虫類に属する動物、及び動物実験委員会が必要と認める動物を用いるすべての実験を審査対象範囲としております(なお、宇宙における動物実験等の場合は、すべての脊椎動物を対象としています)。ただし、すでに終了した実験の結果にかかわるデータ解析については、審査対象外としております。
とくに、資金等に関しては、JAXA と共同研究を実施する他機関の動物実験も含まれますが、その場合においても当該動物実験実施機関による実験計画書の承認書と JAXA の実験計画書を提出していただき、その内容について照合確認をしております。
JAXA 動物実験委員会は、次のように判定を出すこととしております。
- 適正(平成 27 年 3 月までの議事録では「承認」と記載)
- 適正(条件付)(平成 27 年 3 月までの議事録では「条件付承認」と記載)
- 不適(平成 27 年 3 月までの議事録では「否承認」と記載)
(1) 「条件付承認」の場合は、JAXA 動物実験委員会からその理由・条件を示します。実験責任者は、条件を満たすよう実験計画を見直しの上、再度 JAXA 動物実験委員会において条件への適正な対応がなされていることが確認された後でなければ実験を始めることはできません。
(2) 「否承認」の場合は、JAXA 動物実験委員会からその理由・条件を示します。「否承認」であっても、実験計画を見直し、修正した実験計画書を再度提出することを妨げません。実験責任者が委員会の決定に異議がある場合には、異議申し立てを行うことができるものとしております。
注
国際的には、苦痛除去や安楽死に医薬品ではない薬品(試薬や工業用化学物質等)を用いないことがスタンダードになってきていますが、日本は対応が遅れています。
2.アバチン(トリブロモエタノール)
アバチンかつてはマウスの麻酔薬として腹腔内投与により用いられていましたが、現在では下記のような副作用が認められています。
1)特に高用量や高濃度、繰り返しの使用で刺激性があり、腹腔内に投与すると腹膜癒着を起こす可能性がある。特定のマウス系統では、腹腔での炎症により死にいたる重篤な副作用を発生しうるという研究がある。
2)熱で容易に分解し、分解産物は腎臓や肝臓に毒性をもつ。分解したアバチンを投与すると外科手術24時間で死に至る場合がある。
3)投与数週間後に腸閉塞を起こしうる。腸運動を止め、死に至ることもある。またアバチンを光や熱のある場所で貯蔵したり、推奨量や推奨濃度以上で貯蔵すると、より起こしやすくなる。
4)16日齢より幼弱なマウスや炭水化物代謝異常症、例えば糖尿病や肥満のモデルマウスなどは予期しない効果が発生しうる。
アバチンは、現在医薬品として市販されていません。従って麻酔薬として使用する場合は、研究者自ら非医薬品グレードの化学薬品から調整しなければなりません。しかし、麻酔薬等の動物実験に用いる薬品は、研究対象の薬品以外は、医薬品を用いるべきです。
国際的にもアバチンの使用については疑問視されていることから、研究成果の国際ジャーナルへの投稿に際して、アバチンを用いた研究報告は不採択のリスクを伴います。


