OECDのデータ相互受入(MAD)制度とGLP
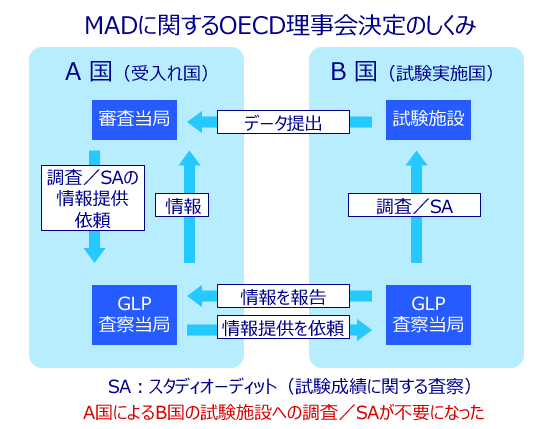
MAD(Mutual Acceptance of Data)とは、データの相互受入のこと。
OECE加盟国およびMAD加盟国の間では、OECDテストガイドラインおよびGLP原則に基づいて行われた非臨床安全性試験のデータの相互受入れ義務があります。データの信頼性は、各国のGLP査察当局が査察評価を行うことによって担保されます。それとは別に、毎年加盟国から4~5カ所を選びGLP査察現地評価を行うことで、加盟国間の調査能力の標準化も図られています。
MADの目的とするところ
- 不要な試験の重複の回避
- 実験動物の使用数削減
- 貿易の円滑化を促進

1981年 理事会決定
MAD(Mutual Acceptance of Data:データの相互受入)について採択されました。
これによって、OECDテストガイドラインおよびGLP原則に基づいて行われた非臨床安全性試験については、その他のOECD加盟国にもデータの受入れの義務が生じることになりました。
1989年 理事会決定
GLP査察実施のために加盟国が遵守すべき事項が定められました。
1997年 理事会決定
OECD非加盟国もMADに参加が可能となりました。
ただし、参加するためには、MADに関する理事会決定を遵守できる能力を示す必要があります。
GLP(Good Laboratory Practice)とは、医薬品、化学物質等の承認申請のために行われる試験のうち、安全性に関わる非臨床試験実施について定められた試験実施規範のこと。非臨床試験には、動物実験(in vivo試験)と非動物実験(in vitro試験、その他)があります。
1970年代に製薬・化学業界でデータ改竄、捏造、省略などの事件が相次いだことへの対策としてアメリカで導入されたのが始まりで、動物福祉を目的としたものではありません。(試験を標準化し「悪い試験」をなくすという意味では無関係ではないですが、独自に福祉的配慮を充実させるような高い自由度はないと考えられています)
1981年にOECDがGLP原則を策定、これをもとに加盟国にGLPの導入を求めたため、日本にも導入されていきました。現在は、4つの省庁がそれぞれを管轄しています(厚生労働省、経済産業省、農水省、環境省)。
1982年:医薬品GLP導入
1984年:化学物質(化審法)GLP導入
農薬GLP導入
1987年:動物用医薬品等GLP導入
1988年:飼料添加物GLP導入
労働安全衛生法GLP導入
2003年:医療機器GLP導入
2014年:再生医療製品等GLP導入
GLP制度では、それぞれに定められた査察実施者が、試験施設ごとに運営管理、試験設備、試験計画、内部監査体制、信頼性保証体制等に関し、適合性を確認します。
参考文献:
第21回GLP研修会(平成27年度)テキスト(公益財団法人日本薬剤師研修センター編集・発行), 2015


